U donoszonego noworodka płci męskiej w drugiej dobie życia wykonano przyłóżkowe badanie ultrasonograficzne płuc celem wstępnej diagnostyki z powodu podejrzenia obecności patologicznej masy w lewym płucu. Podejrzenie wady rozwojowej lewego płuca wysunięto podczas płodowego badania usg wykonanego w trzecim trymetrze ciąży.
Noworodek urodził się w 40 tygodniu ciąży siłami natury w dobrym stanie ogólnym. Po porodzie nie obserwowano zaburzeń oddychania ani innych niepokojących objawów klinicznych.
zawartość artykułu
obrazy ultrasonograficzne
Badanie usg wykonano jako uzupełnienie badania fizykalnego. Do badania wykorzystano głowicę liniową mobilnego aparatu usg Philips Lumify.
Na przedniej powierzchni płuc nie uwidoczniono niepokojących objawów ultrasonograficznych ani patologicznych artefaktów. Objaw ślizgania był obecny nad całą powierzchnią płuc. Obustronnie widoczne były nieliczne artefakty linii Z i I, co uznano za prawidłowy obraz usg płuc u noworodków w pierwszych dobach życia.
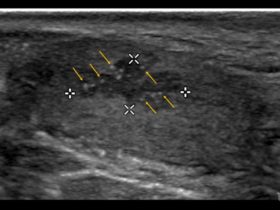
Natomiast na tylnej powierzchni lewego płuca, przykręgosłupowo, na wysokości kąta łopatki uwidoczniono dobrze odgraniczoną, litą zmianę, która była zlokalizowana podopłucnowo.
Podopłucnowa zmiana zlokalizowana w dolnym płacie lewego płuca u noworodka w drugiej dobie życia. Głowica liniowa. Philips Lumify.
Podopłucnowa zmiana zlokalizowana w dolnym płacie lewego płuca u noworodka w drugiej dobie życia. Głowica liniowa. Philips Lumify.
Zmiana miała nieco niejednorodną echogeniczność, a w jej świetle widoczne były drobne obszary płynowe. Nie uwidoczniono cech bronchogramu powietrznego. Zmiana zachowywała ruchomość oddechową.
Niejednorodna echogeniczność zmiany podopłucnowej z widocznymi obszarami płynowymi. Głowica liniowa. Philips Lumify.
Widoczna zachowana ruchomość oddechowa zmiany zlokalizowanej podopłucnowo. Głowica liniowa. Philips Lumify.
W opcji kolorowego dopplera uwidoczniono pojedyncze naczynie tętnicze z silnym sygnałem, doprowadzające krew do zmiany z aorty piersiowej.
Naczynie tętnicze pochodzące z aorty piersiowej i doprowadzające krew do patologicznej zmiany zlokalizowanej podopłucnowo. Głowica liniowa. Philips Lumify.
W opcji kolorowego dopplera widoczne jest pojedyncze naczynie doprowadzające krew z aorty piersiowej do zmiany podopłucnowej. Głowica liniowa. Philips Lumify.
rozpoznanie
Sekwestracja płucna wewnątrzpłatowa
czym jest sekwestracja płucna?
Sekwestracja płucna jest wadą rozwojową układu oddechowego polegającą na nieprawidłowym rozwoju fragmentu tkanki płucnej, najczęściej pozbawionej łączności z drzewem oskrzelowym i unaczynionej z naczyń pochodzących z krążenia systemowego.
Sekwestracja stanowi około 6% wrodzonych wad układu oddechowego i występuje u około 1,8% populacji ogólnej.
Wyróżnia się dwa główne typy sekwestracji płucnej:
- wewnątrzpłatowa
- zewnąrzpłatowa.
Sekwestracja zewnątrzpłatowa może być zlokalizowana w klatce piersiowej lub podprzeponowo.
Sekwestracja wewnątrzpłatowa:
- fragment nieprawidłowej tkanki jest wkomponowany w miąższ zdrowego płuca i pokrywa go wspólna opłucna
- stanowi 75-85% wszystkich przypadków sekwestracji
- najczęściej lokalizuje się w dolnym płacie lewego płuca (60%)
- może mieć zachowaną łączność z drzewem oskrzelowym
- unaczynienie pochodzi z naczyń systemowych, najczęściej z aorty
- spływ żylny uchodzi do żył płucnych
- zwykle jest izolowaną wadą
- występuje z równą częstością u obu płci
- rzadko daje objawy kliniczne w pierwszych latach życia
- może być przyczyną nawracających zapaleń płuc
Sekwestracja zewnątrzpłatowa:
- rozwija się poza prawidłowym płucem
- jest pokryta własną opłucną
- najczęściej lokalizuje się między dolnym płatem lewego płuca a przeponą
- w 10-15% ma lokalizację podprzeponową
- zazwyczaj nie ma połączenia z drzewem oskrzelowym
- unaczynienie tętnicze i żylne jest pochodzenia systemowego
- w 60% wiąże się z obecnością dodatkowych wad rozwojowych (m.in. przepuklina przeponowa, wady serca, wady przewodu pokarmowego)
- występuje czterokrotnie częściej u mężczyzn
- objawy kliniczne pojawiają się w pierwszych miesiącach życia (m.in. cechy niewydolności oddechowej, krążeniowej, trudności w karmieniu)
obraz ultrasonograficzny sekwestracji płucnej
W obrazie ultrasonograficznym sekwestracja płucna ma charakter litej zmiany o echogeniczności wyższej niż miąższ płuca. W jej świetle mogą być obecne obszary płynowe. W badaniu usg wykonywanym podczas ciąży jest najczęściej hiperechogeniczna. Sekwestracja płucna może mieć bogate unaczynienie w opcjach dopplerowskich, co wynika z systemowego pochodzenia naczyń doprowadzających krew do zmiany.
Cechą charakterystyczną sekwestracji płucnej jest obecność naczynia tętniczego doprowadzającego krew do zmiany z silnym sygnałem dopplerowskim. Naczynie to najczęściej wychodzi z aorty.
Naczynie tętnicze wychodzące z aorty piersiowej i doprowadzające krew do sekwestracji płucnej wewnątrzpłatowej u noworodka. Głowica liniowa. Philips Lumify.
diagnostyka różnicowa
- gruczolakowatość torbielowata płodu (cystic adenomatoid malformation),
- wrodzona rozedma miąższu płucnego,
- wady serca,
- wrodzona przepuklina przeponowa,
- przetoka tchawiczo-przełykowa,
- torbiele oskrzelopochodne
- choroby rozrostowe, głównie neuroblastoma
PHILIPS LUMIFY w portalu eduson.pl
Zobacz pozostałe obrazy ultrasonograficzne zarejestrowane głowicami PHILIPS LUMIFY.
Zobacz jak wykorzystać głowicę konweksową PHILIPS LUMIFY?
- Ostre zapalenie pęcherzyka żółciowego
- Wodobrzusze
- Obrzęk płuc w przezklatkowym badaniu usg płuc na wizycie domowej
- Przetoka wrotno-systemowa
- Czy to możliwe, aby korzystając z ultrasonografu mieszczącego się kieszeni, uwidocznić w moczowodzie złóg z artefaktem migotania?
- Krwawienie do nadnerczy u noworodków
- Kamica pęcherzyka żółciowego u dzieci
- Rak trzustki i głowica Lumify
- Obrazy ultrasonograficzne wątroby w głowicy Lumify
- Obrazy ultrasonograficzne pęcherzyka żółciowego w głowicy LUMIFY
- Pacjent z dusznością i głowica PHILIPS LUMIFY
- Czy w przezbrzusznym badaniu usg można uwidocznić zmianę w ścianie żołądka?
- Ultrasonograficzny „trik” – zobacz, jak z jednego przyłożenia głowicy do wątroby uzyskać maksimum informacji
- Ogniskowy rozrost guzkowy (ang. FNH, focal nodular hyperplasia) u dzieci
- Czy ultrasonograf zastąpi stetoskop?
- Czy zawsze wiesz, gdzie szukać pęcherzyka żółciowego? Nie daj się zaskoczyć!
- Liniowa czy konweksowa – którą głowicę wybrać do obrazowania płuc?
Jak wykorzystać głowicę liniową PHILIPS LUMIFY?
- Ciało obce (drzazga)
- Węzły chłonne krezkowe
- Odma opłucnowa
- Wrzodziejące zapalenie jelit
- Przerzuty raka migdałka podniebiennego do węzłów chłonnych szyjnych
- Zespół Sjogrena – obraz ultrasonograficzny ślinianek
- Kaszel, gorączka i ultrasonografia. Czy zapalenie płuc widać w usg?
- Rola USG we wstępnej diagnostyce złamań kości długich
- Zapalenie uchyłków jelita grubego
- Torbiel podwyściółkowa czy torbiel w splocie naczyniówkowym? A może to jedno i to samo?
- Choroba Castlemana ślinianki przyusznej
- Jak znaleźć wyrostek robaczkowy?
- Biopsja tarczycy u dziecka
- Choroba Gravesa i Basedowa – obraz ultrasonograficzny
- USG nerwu wzrokowego w podejrzeniu podwyższonego ciśnienia śródczaszkowego
- Guz w ścianie jamy brzusznej lub klatki piersiowej. Spektrum obrazów ultrasonograficznych.
- Ginekomastia u nastolatka
- Czy ten guz na szyi to torbiel środkowa? Sprawdź sam!
- Zakrzepica żył głębokich kończyn dolnych – point of care
- Choroba Hashimoto u dziecka
- BACC zmiany ogniskowej tarczycy – aktualne rekomendacje
- Jakie cechy prawidłowych węzłów chłonnych szyjnych są najważniejsze?
- USG płuc – jak poprawnie ustawić aparat usg?
- Dziewczynka z wyczuwalnym guzkiem okolicy podbrzusza i nawracającymi bólami brzucha
- Mikrolitiaza jąder
- Ropień sutka
- Ultrasonografia przepony
- Powiększenie moszny u 2-letniego pacjenta
- Jak w badaniu usg udokumentować reakcję źrenicy na światło?
- „Żabka” w badaniu usg
- Kanał pachwinowy w obrazach usg
- Pomiar grubości kompleksu błony środkowej i wewnętrznej tętnicy szyjnej (intima-media complex thickness)
Zacznij przygodę z PHILIPS LUMIFY – to proste!
Zajrzyj na stronę PHILIPS LUMIFY i sprawdź aktualne promocje.
Na stronie PHILIPS LUMIFY znajdziesz także opisy przypadków i wykłady na temat ultrasonografii płuc.
piśmiennictwo
- Winters WD, Effmann EL. Congenital masses of the lung: prenatal and postnatal imaging evaluation. J Thorac Imaging. 2001 Oct;16(4):196-206. [Medline]
- Abbey P, Das CJ, Pangtey GS, Seith A, Dutta R, Kumar A. Imaging in bronchopulmonary sequestration. J Med Imaging Radiat Oncol. 2009 Feb;53(1):22-31. [Medline]
- Corbett HJ, Humphrey GM. Pulmonary sequestration. Paediatr Respir Rev. 2004 Mar;5(1):59-68. [Medline]
- Chowdhury MM, Chakraborty S. Imaging of congenital lung malformations. Semin Pediatr Surg. 2015 Aug;24(4):168-75. [Medline]
- Mazurek H, Buchwald J, Pogorzelski A. Sekwestracja płucna. Pediatr Dypl. 2013;17(1):56-60.