zawartość artykułu
Wstęp
Naczyniakomięśniakotłuszczak (angiomyolipoma AML) jest łagodnym guzem nerki zaliczanym do grupy PEComa (perivascular epithelioid cell tumors) [1]. Naczyniakomięśniakotłuszczak utworzony jest z tkanki tłuszczowej, komórek mięśni gładkich i naczyń krwionośnych. Zależnie od zawartości tkanki tłuszczowej wyróżnia się następujące podtypy:
- klasyczny AML (classic angiomyolipoma)
- AML z małą zawartością tkanki tłuszczowej (fat poor angiomyolipoma)
AML może być guzem występującym sporadycznie, bądź w przebiegu stwardnienia guzowatego (SG) [2,3]. AML występujący sporadycznie najczęściej jest pojedynczą zmianą, czterokrotnie częściej występuje u płci żeńskiej [4]. AML u pacjentów z SG są najczęściej zmianami mnogimi, małymi, występującymi obustronnie, z porównywalną częstotliwością u obojga płci [2,3]. Uważa się, że u do 80% chorych z SG będzie widoczna więcej niż jedna zmiana o charakterze AML [2,4].
Obrazy ultrasonograficzne
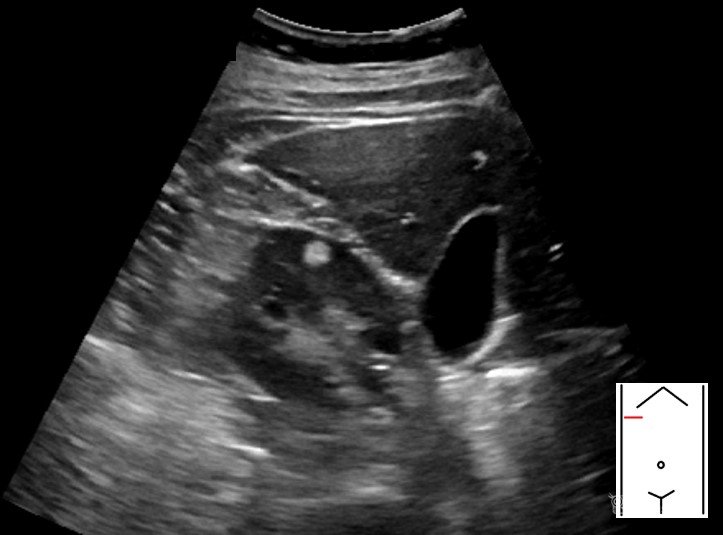
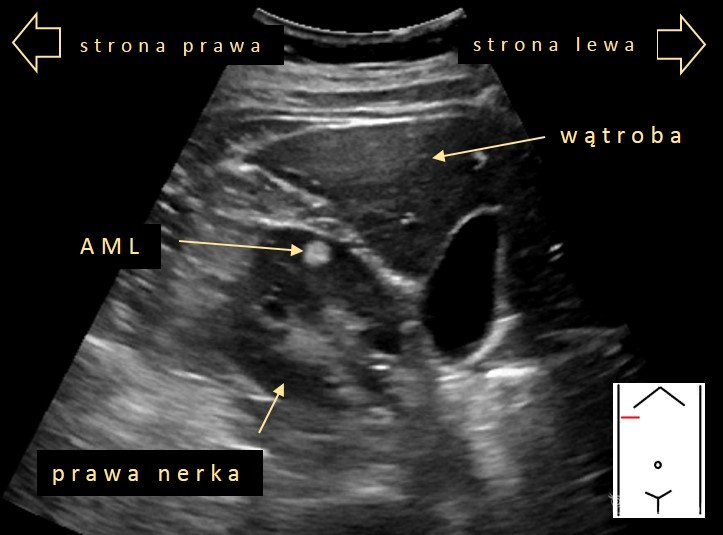
AML (angiomyolipoma) w badaniu ultrasonograficznym najczęściej jest zmianą litą, hiperechogeniczną (95%), dobrze ograniczoną, jednorodną (68-90%), okrągłego kształtu, położoną w miąższu nerki [5,6,7,8]. W około 25% przypadków AML położony jest egzofitycznie [9]. Ze względu na różnicę echogeniczności pomiędzy AML a korą nerki, zmiany nawet o średnicy kilku milimetrów są dobrze widoczne [5].
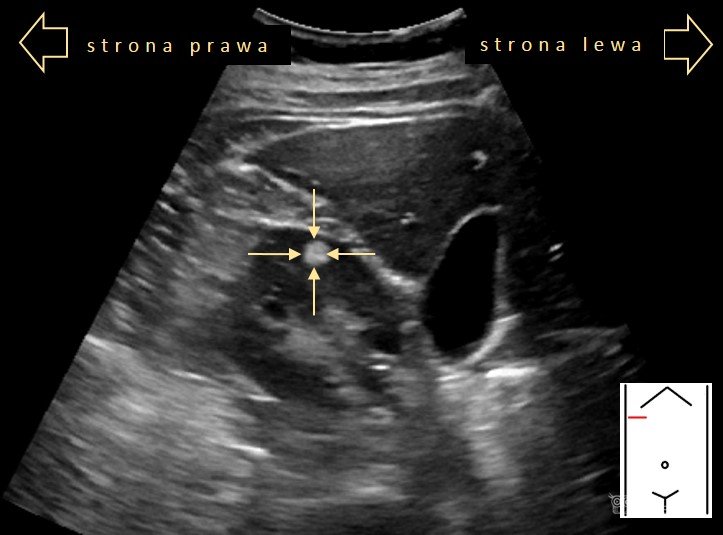
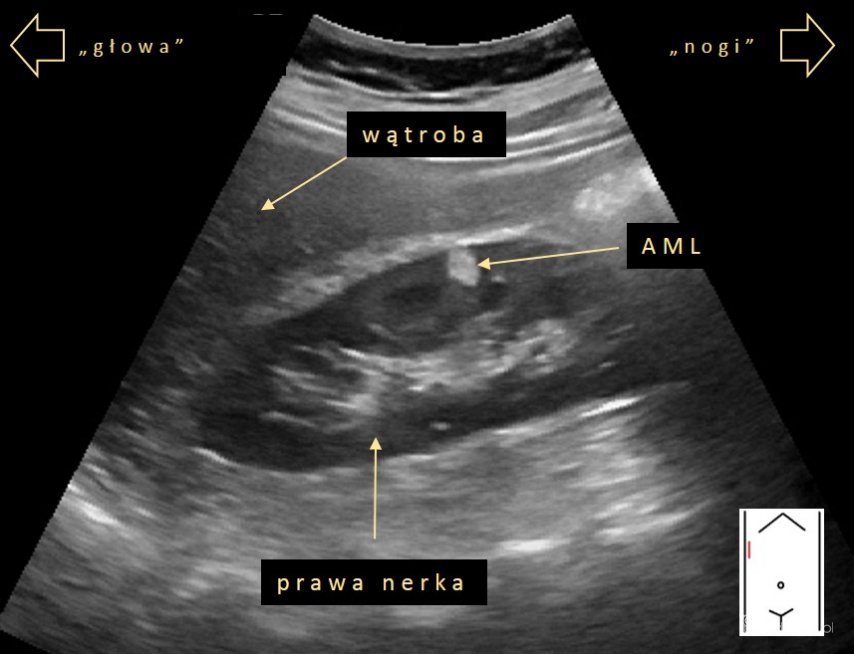
AML prawej nerki.
AML prawej nerki. Włączona opcja dopplera mocy.
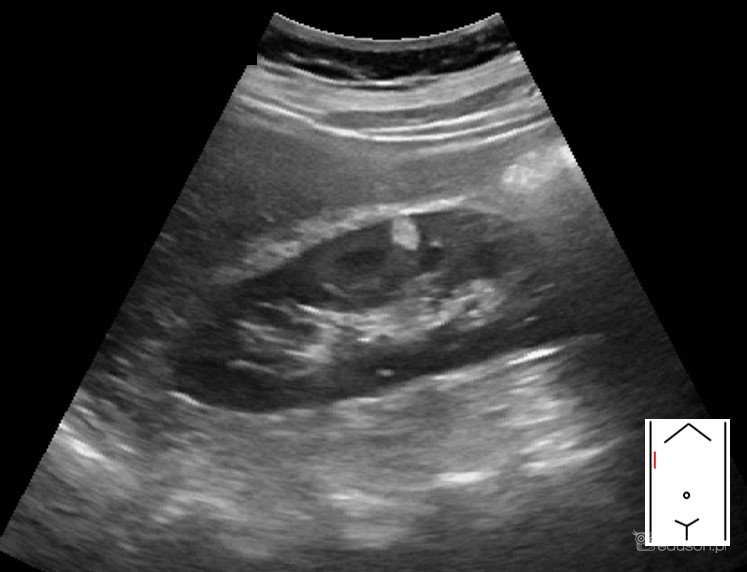
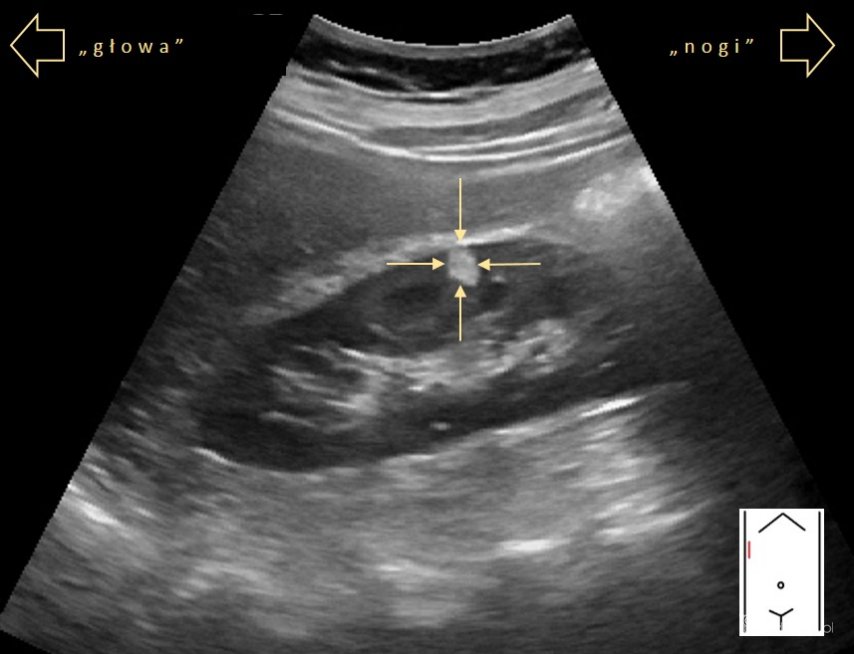
AML prawej nerki.
Normoechogenicze i hiopoechogeniczne – tzw. nietypowe AML – występują zdecydowanie rzadziej (ok 5% AML) niż hiperechogeniczne i związane jest to mniejszą zawartością tkanki tłuszczowej [6,10]. Obszary płynowe, będące następstwem martwicy lub krwawienia do zmiany, bardzo rzadko widoczne są w AML. Jeżeli występują, to z reguły w przypadku dużych (powyżej 4 cm średnicy) AML. W przypadku AML w przebiegu SG obserwuje się – w porównianiu do sporadycznego AML – zwiększanie się wymiarów zmiany: 18% vs 5% [11]. Ponadto w AML w przebiegu SG opisywano przypadki krwawienia do guza, podczas gdy w sporadycznym AML krwawienia występują rzadko [3].
Aspekty praktyczne badania ultrasonograficznego
AML (angiomyolipoma) a rak nerki – RCC (renal cell carcinoma)
Rozróżnienie pomiędzy AML a niewielkim hiperechogenicznym RCC w badaniu ultrasonograficznym może być trudne. W badaniu ultrasonograficznym ważne jest zwrócenie uwagi na następujące elementy:
- ocena zarysów zewnętrznych – w przypadku AML granice są gładkie i zmiana jest dobrze ograniczona [5]
- cień akustyczny poniżej – może być widoczny w przypadku niektórych AML, nie był natomiast opisywany w rakach nerki. Cień akustyczny poniżej AML widoczny może być w 20-34% przypadków [6].
- AML są częściej zmianami jednorodnymi (68-90%). Rak nerki jest częściej niejednorodny (65-76%). Obszary płynowe zdecydowanie częściej występują w przebiegu raka nerki – 12-53% [6].
- obecność bezechowego „halo” wokół zmiany częściej obserwowane było w rakach niż w AML.
Do pewnego rozpoznania konieczne jest badanie TK lub MRI, celem identyfikacji tkanki tłuszczowej. Jednakże należy pamiętać, że poniżej 5% AML może nie zawierać tłuszczowej lub zawierać jej bardzo małą objętość (fat poor angiomyolipoma), z kolei rak jasnokomórkowy nerki i guz Wilmsa mogą niekiedy zawierać tkankę tłuszczową [5]. Ponadto należy mieć na uwadze możliwość synchronicznego (jednoczasowego) występowania AML i raka nerki. Sytuacja taka w badaniu McBlunt i wsp. była obserwowana była u 7% pacjentów z AML bez SG [12]. Dlatego ważna jest czujność onkologiczna u osób zgłaszających się na kontrolne badaniu ultrasonograficzne AML: w przypadku pojawienia się kolejnej hiperechogenicznej zmiany należy uwzględnić w diagnostyce różnicowej synchronicznego raka nerki. W badaniu Sidhar i wsp. 29% raków nerki o średnicy mniejszej niż 2cm zakwalifikowano jako zmiany hiperechogeniczne (echogeniczność porównywalną do echogeniczności echa centralnego nerki). Natomiast w grupie raków nerki o średnicy powyżej 3cm; zmiany hiperechogeniczne stanowiły 4% [13].
AML (angiomyolipoma) – średnica zmiany w kontrolnych badaniach ultrasonograficznych
Lemaitre i wsp. obserwowali zwiększanie się wymiarów AML u pacjentów podzielonych na 3 grupy:
- pojedynczy AML;
- mnogie AML niezwiązane z SG;
- mnogie AML związane z SG.
Obserwowano zwiększanie się wymiarów (powierzchni) AML w kontrolnych badaniach ultrasonograficznych i tomografii komputerowej, rocznie odpowiednio dla każdej z grup o: 5%; 22%; 18%. W grupie 1. i 2. w kontrolnych badaniach obserwowano także zwiększenie się liczby zmian [11].
Podsumowanie
Nie każda zmiana hiperechogeniczna w nerce to AML. Obraz ultrasonograficzny raka nerki (RCC) może przypominać AML. Należy także pamiętać o możliwości wystąpienia synchronicznego AML i raka nerki. Różnicując AML z rakiem nerki na podstawie obrazu ultrasonograficznego, poza oceną echogeniczności, uwagę należy zwrócić na:
- cień akustyczny za guzem (w około 21-33% AML; bardzo rzadko w raku nerki);
- bezechowy pierścień wokół zmiany (w około 73% raków nerki; rzadko w AML);
- obszary płynowe (w około 31% raków nerki; rzadko w AML).
W przypadku licznych AML należy rozważyć obserwację w kierunku SG, jeżeli dotychczas diagnostyka w tym kierunku nie była prowadzona.
Piśmiennictwo
- Prasad SR, Sahani DV, Mino-Kenudson M, Narra VR, Humphrey PA, Menias CO, Chintapalli KN. Neoplasms of the perivascular epithelioid cell involving the abdomen and the pelvis: cross-sectional imaging findings. J Comput Assist Tomogr. 2007 Sep-Oct;31(5):688-96.[Medline]
- Rumack CM, Wilson SR, Charboneu JW. Levine D. Diagnostic Ultrasond. Wyd IV.2011. Mosby,Elsevier.
- Jinzaki M, Silverman SG, Akita H, Nagashima Y, Mikami S, Oya M. Renal angiomyolipoma: a radiological classification and update on recent developments in diagnosis and management. Abdom Imaging. 2014 Jun;39(3):588-604. [Medline] [Full text]
- Prasad SR, Surabhi VR, Menias CO, Raut AA, Chintapalli KN. Benign renal neoplasms in adults: cross-sectional imaging findings. AJR Am J Roentgenol. 2008 Jan;190(1):158-64.[Medline] [Full text]
- Bates JA. Abdominal Ultrasound. How, Why, and When. Wyd. II. 2004, Elsevier Limited
- Lewicki A, Jakubowski W, Lewicka A, Jędrzejczyk M. Ultrasonograficzny atlas zmian ogniskowych nerek. Roztoczańska Szkoła Ultrasonografii. Wyd I. Warszawa-Zamość 2011.
- Yamashita Y, Ueno S, Makita O, Ogata I, Hatanaka Y, Watanabe O, Takahashi M. Hyperechoic renal tumors: anechoic rim and intratumoral cysts in US differentiation of renal cell carcinoma fromangiomyolipoma. Radiology. 1993 Jul;188(1):179-82. [Medline]
- Jinzaki M, Ohkuma K, Tanimoto A, Mukai M, Hiramatsu K, Murai M, Hata J. Small solid renal lesions: usefulness of power Doppler US. Radiology. 1998 Nov;209(2):543-50. [Medline]
- Stella Sy Ho. Renal Angiomyolipoma. W Ahuja AT red. Diagnostic Imaging Ultrasound. Amirsys Wyd. I. 2007.
- Jinzaki M, Tanimoto A, Narimatsu Y, Ohkuma K, Kurata T, Shinmoto H, Hiramatsu K, Mukai M, Murai M. Angiomyolipoma: imaging findings in lesions with minimal fat. Radiology. 1997 Nov;205(2):497-502. [Medline]
- Lemaitre L, Robert Y, Dubrulle F, Claudon M, Duhamel A, Danjou P, Mazeman E. Renal angiomyolipoma: growth followed up with CT and/or US. Radiology. 1995 Dec;197(3):598-602.[Medline]
- Blute ML, Malek RS, Segura JW. Angiomyolipoma: clinical metamorphosis and concepts for management. J Urol. 1988 Jan;139(1):20-4. [Medline]
- Sidhar K, McGahan JP, Early HM, Corwin M, Fananapazir G, Gerscovich EO. Renal Cell Carcinomas: Sonographic Appearance Depending on Size and Histologic Type. J Ultrasound Med. 2016 Feb;35(2):311-20. [Med line]